Luis Ricciardi 1 , Rosa Mazzeo 2,*© , angelo raffaele marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Ioviano 4 , Vito Zonno 1 , Stefano Paván 1 © y Concetta Lotti 2,*
- 1 Departamento de Ciencias del Suelo, Plantas y Alimentos, Unidad de Fitomejoramiento y Genética Vegetal Universidad de Bari, Via Amendola 165/A, 70125 Bari, Italia; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (BRAZO); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Departamento de Ciencias de la Agricultura, Alimentación y Medio Ambiente, Universidad de Foggia, Via Napoli 25, 71122 Foggia, Italia
- 3 Departamento de Biociencias, Biotecnologías y Biofarmacéuticos, Universidad de Bari, Via Orabona 4, 70125 Bari, Italia; guglielmo.rainaldi@uniba.it
- 4 Departamento de Tecnologías Energéticas, División de Bioenergía, Biorrefinería y Química Verde, Centro de Investigación ENEA Trisaia, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italia; paolo.iovieno@enea.it
* Correspondencia: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Abstracto:
Cebolla (Allium cepa L.) es el segundo cultivo vegetal más importante a nivel mundial y es ampliamente apreciado por sus beneficios para la salud. A pesar de su importante importancia económica y su valor como alimento funcional, la cebolla ha sido poco investigada con respecto a su diversidad genética. En este documento, investigamos la variación genética en la “cebolla roja Acquaviva” (ARO), una raza local con una historia centenaria de cultivo en un pequeño pueblo de la provincia de Bari (Apulia, sur de Italia). Se utilizó un conjunto de 11 marcadores de microsatélites para explorar la variación genética en una colección de germoplasma que constaba de 13 poblaciones ARO y tres tipos comerciales comunes. Los análisis de la estructura genética con métodos paramétricos y no paramétricos destacaron que el ARO representa un acervo genético bien definido, claramente distinto de las razas locales Tropea y Montoro con las que a menudo se confunde. Con el fin de brindar una descripción de los bulbos, generalmente utilizados para consumo en fresco, se evaluó el contenido de sólidos solubles y la acritud, mostrando mayor dulzura en el ARO con respecto a las dos razas locales mencionadas anteriormente. En general, el presente estudio es útil para la valorización futura de la ARO, que podría promoverse a través de etiquetas de calidad que podrían contribuir a limitar los fraudes comerciales y mejorar los ingresos de los pequeños agricultores.
Introducción
El género Allium incluye alrededor de 750 especies [1], entre las cuales la cebolla (Allium cepa L., 2n = 2x =16) es una de las más extendidas. A. cepa tiene un ciclo bienal y un comportamiento reproductivo cruzado. En la actualidad, la producción mundial de cebolla (97.9 Mt) la convierte en el segundo cultivo hortícola más importante después del tomate [2]. Desde la antigüedad, los bulbos de cebolla se han utilizado como alimento y en aplicaciones medicinales populares. De hecho, los antiguos egipcios ya reportaron varias fórmulas terapéuticas basadas en el uso de ajo y cebolla en un papiro médico del 1550 aC, el Codex Ebers [3].
Este vegetal versátil y saludable se consume crudo, fresco o como producto procesado y se utiliza para realzar el sabor de muchos platos. Varios estudios recientes afirman que el consumo de cebolla puede reducir el riesgo de enfermedades cardiovasculares [4,5], obesidad [6], diabetes [7] y diversas formas de cáncer [8–10]. Las propiedades saludables de la cebolla a menudo se atribuyen a los altos niveles de dos clases de compuestos nutracéuticos: flavonoides y sulfóxidos de alqu (en) il cisteína (ACSO). La primera clase incluye flavonoles y antocianinas. La quercetina es el principal flavonol detectable, conocido por sus fuertes propiedades antioxidantes y antiinflamatorias en la eliminación de radicales libres y la unión de iones de metales de transición. [ 11 ]; mientras que las antocianinas confieren color rojo/morado a algunas variedades de cebolla. En cuanto a los ACSO, el más abundante es la isoalina [(+)-trans-S-1-propenil-L-cisteína sulfóxido] [ 12 ], un aminoácido azufrado no volátil y no proteinogénico almacenado en las células, que es indirectamente responsable del aroma y sabor picante de las cebollas [ 13 ]. Tras la ruptura del tejido, la isoallina es escindida por la enzima alinasa para producir una serie de compuestos volátiles (piruvato, amoníaco, tiosulfonatos y óxido S de propano) que inducen lagrimeo y causan un olor desagradable (acre) [ 14 ]. La acritud de la cebolla a menudo se mide como la cantidad, por gramo de peso fresco, de ácido pirúvico generado por hidrólisis. [15, 16].
En los países de la cuenca mediterránea, propuesto como uno de los centros secundarios de diversidad de A cepa [17, 18], los bulbos de cebolla muestran una amplia variabilidad en forma, tamaño, color, materia seca y acritud [19-dieciséis]. Además, la fertilización a base de azufre, las prácticas agronómicas, el tipo de suelo, las condiciones climáticas y el genotipo de los cultivares o variedades locales pueden influir en la calidad del bulbo al conferir valores organolépticos y nutricionales peculiares. [23-dieciséis]. En Italia, a pesar de la amplia disponibilidad de germoplasma de cebolla, solo unas pocas variedades de cebolla a menudo se someten a estudios científicos y se caracterizan adecuadamente. [28, 29].
La caracterización genética y fenotípica minuciosa de la agrobiodiversidad es crucial para asegurar la conservación adecuada de los recursos fitogenéticos y promover el uso de genotipos específicos en la cadena de valor. [30-dieciséis]. Los marcadores de repetición de secuencia simple (SSR) se han elegido a menudo para mapear [33-dieciséis], huellas dactilares de ADN y discriminación de cultivares [36-dieciséis], y estimación confiable de la variabilidad genética dentro y entre razas locales [39-dieciséis], ya que son específicos de locus, multialélicos, heredados codominantemente, altamente reproducibles y adecuados para el genotipado automatizado.
En el presente estudio, centramos nuestra atención en una variedad autóctona tradicional de Apulia, la “cebolla roja de Acquaviva” (ARO), que se cultiva según métodos de agricultura biológica en una pequeña zona de la ciudad de Acquaviva delle Fonti, en la provincia de Bari. (Apulia, sur de Italia). Los bulbos de esta variedad autóctona son grandes, aplanados y de color rojo y se utilizan mucho en las recetas locales. Aunque la ARO obtuvo la marca de calidad “Slow Food Baluarte”, su producción podría ser promovida y protegida aún más por las marcas de calidad de la Unión Europea, como la indicación geográfica protegida (IGP) y la denominación de origen protegida (POD), ya que podrían contribuir a limitar la fraudes comerciales y mejorar los ingresos de los pequeños agricultores. En este documento, los marcadores moleculares SSR se utilizaron como herramientas poderosas para evaluar la variación genética entre las poblaciones ARO y para discriminar esta variedad local de otras dos variedades locales de cebolla roja del sur de Italia. Además, estimamos la pungencia y el contenido de sólidos solubles para evaluar el sabor de ARO en relación con la demanda del mercado.
Resultados
Establecimiento de la Colección de Germoplasma de Cebolla Roja Acquaviva y Caracterización Morfológica
Se utilizaron semillas de 13 poblaciones de la variedad autóctona ARO, donadas por agricultores en el marco del proyecto BiodiverSO Apulia Region, para establecer una colección de germoplasma ARO.
Los descriptores morfológicos, relacionados con el bulbo, la piel y la pulpa, se recolectaron en germoplasma ARO y en tres razas criollas de cebolla, dos pertenecientes a la raza criolla “Cebolla roja Tropea” (TRO) y una a la raza criolla “Cebolla cobre Montoro” (MCO) (Figura 1). Todos los bulbos ARO eran planos y se caracterizaban por una piel externa roja y pulpa con diferentes tonalidades de rojo. En contraste, la pulpa de los bulbos TRO era completamente roja, mientras que la pulpa de los bulbos MCO estaba pobremente pigmentada (Tabla S1). El análisis bioquímico permitió evaluar el contenido de sólidos solubles y la pungencia. Como se informa en la Tabla 1, los valores medios del contenido de sólidos solubles de los bulbos en poblaciones ARO fue de 7.60, y varió de 6.00 (ARO12) a 9.50° Brix (ARO11 y ARO13). Este valor fue superior al estimado para las razas criollas TRO y MCO (4.25 y 6.00° Brix, respectivamente).

Tabla 1. Contenido de sólidos solubles y valores de pungencia evaluados en las poblaciones de “Cebolla Roja Acquaviva” (ARO), “Cebolla Roja Tropea” (TRO) y “Cebolla Cobre Montoro” (MCO) *.
| CÓDIGO | Contenido de sólidos solubles (Brix) | pungencia (pmoldear–1 adelante) | ||
| Media | CV y (%) | Media | CV y (%) | |
| ARO1 | 6.25D * | 5.65 | 5.84ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 la | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28/XNUMX/XNUMX desde | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 la | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 la | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51/XNUMX/XNUMX desde | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25/XNUMX/XNUMX desde | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 la | 3.49 |
| ARO9 | ABC 8.25 | 4.28 | 6.84 la | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94/XNUMX/XNUMX desde | 6.57 |
| ARO11 | 9.50 A | 7.44 | 5.54/XNUMX/XNUMX desde | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91/XNUMX/XNUMX desde | 9.70 |
| ARO13 | 9.50 A | 7.44 | 6.63 la | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18/XNUMX/XNUMX desde | 2.66 |
| TRO1 | E 4.25 | 8.31 | 2.80 b | 2.10 |
| TRO2 | E 4.25 | 8.31 | 4.28/XNUMX/XNUMX desde | 4.79 |
* Medias con las mismas letras en mayúsculas o minúsculas no son estadísticamente diferentes a 0.01P o 0.05P, respectivamente (Test de SNK). y Coeficiente de variación.
El valor medio de pungencia ARO, evaluado por medio del contenido de ácido pirúvico, fue de 6.00, osciló entre 4.51 pmol g-1 FW (ARO6) a 7.04 (ARO8). Este valor fue superior al estimado en las razas TRO y MCO (3.54 pmol g-1 FW y 4.18 pmol g-1 FW, respectivamente).
Polimorfismo SSR y relaciones genéticas entre accesiones
En el presente estudio, 11 de las 37 combinaciones de cebadores SSR probadas proporcionaron polimorfismos de un solo locus, es decir, produjeron como máximo dos productos de amplificación en un solo individuo. En general, se detectaron 55 alelos en 320 individuos con un número de alelos por locus que va de 2 (ACM147 y ACM 504) a 11 (ACM132) y un valor medio de 5 alelos (Tabla 2). En poblaciones individuales, el número de alelos (Na) osciló entre 1.94 (ACM147 y ACM504) y 5.38 (ACM132), mientras que el número efectivo de alelos (Ne) osciló entre 1.41 (ACM152) y 2.82 (ACM449). discrepancias entre los valores de Na y Ne se debieron a la presencia de alelos con baja frecuencia en las poblaciones y al predominio de pocos alelos. El valor de heterocigosis (Ho) más alto observado se destacó para ACM138 y ACM449 (0.62), mientras que el más bajo se asoció con ACM152 (0.25). La heterocigosidad esperada (He), que corresponde a la expectativa teórica en una población panmíctica, osciló entre 0.37 (ACM504) y 0.61 (ACM132, ACM138 y ACM449). El índice de fijación de Wright (Fis), mostró valores cercanos a cero (promedio 0.05) para todos los marcadores, indicando valores similares entre los niveles de heterocigosis observados y esperados, como se esperaba para una especie cruzada. La eficiencia del marcador SSR individual en la huella genética se estimó mediante el índice de contenido de información polimórfica (PIC), con un valor medio de 0.48 y varió de 0.33 (ACM504) a 0.67 (ACM132). Otro índice de eficiencia, el índice de información de Shannon (I) mostró un valor medio de 0.84 y los valores asumidos oscilaron entre 0.45 (ACM152) y 1.20 (ACM132).
Tabla 2. Características de polimorfismo de los 11 marcadores SSR utilizados para estimar la diversidad genética en poblaciones ARO, TRO y MCO. Número total de alelos (Na), rango de tamaño de banda e índice de contenido de información polimórfica (PIC) Consulte el conjunto total de 320 individuos genotipados en este estudio. Número de alelos (Na), número de alelos efectivos (Ne), heterocigosidad observada (Ho), heterocigosidad esperada (He), índice de fijación (Fis), y el índice de información de Shannon (I) se refieren a valores medios calculados a partir de 16 poblaciones, cada una compuesta por 20 individuos.
| Lugar. | Na total | Rango de tamaño (pb) | PIC | Media | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189 - 205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229 - 241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186 - 248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242 - 272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264 - 266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228 - 244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286 - 298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108 - 120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120 - 140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202 - 210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188 - 192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Media | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Entre las poblaciones, ARO3, ARO6, ARO8, ARO10, TRO1 y MCO mostraron un alto nivel de variación genética (Ho > 0.5), mientras que la diversidad más baja se observó en la población ARO7 (Ho = 0.27) (Tabla complementaria S2). En general, todas las accesiones exhibieron Fis valores cercanos a cero (Fis valor medio = 0.054), como se esperaba en condiciones de apareamiento aleatorio.
Análisis de Varianza Molecular y Estructura Genética
AMOVA calculó la partición jerárquica de la variación genética entre y dentro de las poblaciones. Los resultados destacaron una fracción considerable de variación genética dentro de las poblaciones (87%). La variación entre poblaciones, 13%, fue altamente significativa (P < 0.001) (Tabla 3). Los valores por pares del parámetro Fpt, un análogo del índice de fijación Fst de Wright, que van de 0.002 (ARO2/ARO10) a 0.468 (ARO7/TRO2), fueron significativos (P <0.05), excepto por nueve comparaciones por pares (Tabla complementaria S3).
Tabla 3. Análisis de Varianza Molecular de 320 Genotipos de 16 Poblaciones de Allium cepa L.
| Fuente | df | Suma de cuadrados | Estimación de varianza | Varianza (%) | Fpt | P |
| Entre poblaciones | 15 | 458.63 | 1.16 | 13% | ||
| Dentro de las poblaciones | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Total | 319 | 2731.62 | 8.66 |
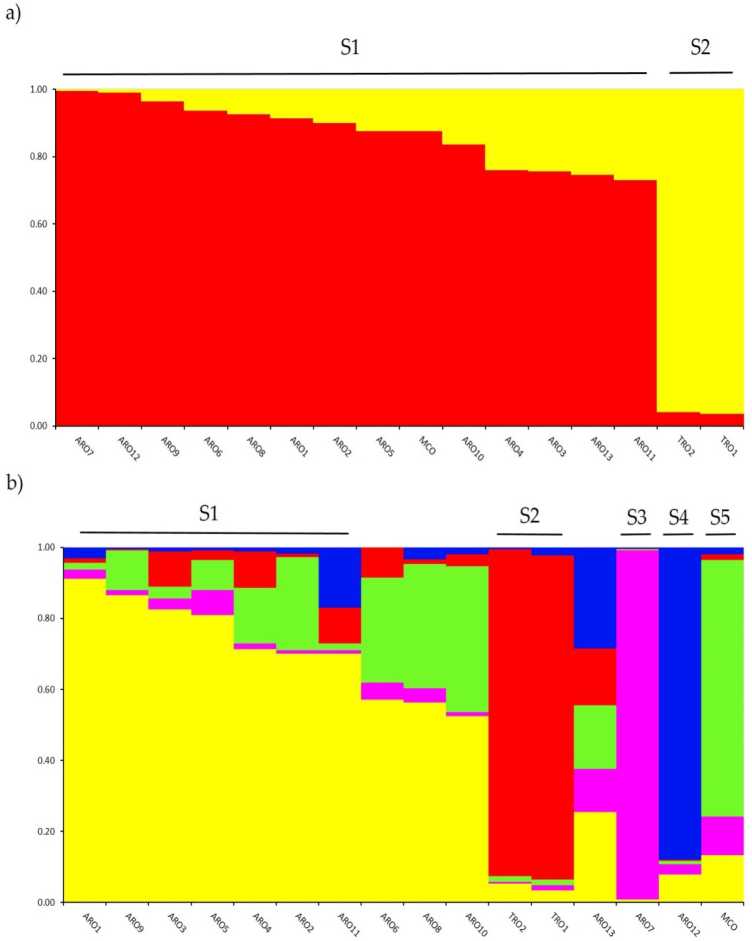
Investigación de la estructura genética en el A cepa La colección genotipada en este estudio se realizó mediante el análisis de agrupamiento basado en el modelo de mezcla implementado en el software STRUCTURE. El método Evanno AK sugirió la subdivisión en dos grupos (K = 2) como el más informativo para nuestro datos,con the Next PE más altoAk en K = 5 (régimen complementario S1). La tenedor = 2, ahpopulaciones waquí el culoigned tambiénny elf los dos racimos un coeficiente de rnernbertoip (q) > 0.7. como shown en Figura 2a, el primer grupo (denominado S1) incluía MCO y todas las poblaciones ARO, mientras que el grupo S2 agrupaba las dos poblaciones TRO. En K = 5, proporcionando una descripción más profunda del conjunto de datos (Figura 2b), el 75% de las accesiones se asignaron a uno de los cinco conglomerados. Se confirmó la separación entre ARO (S1) y TRO (S2), aunque algunas poblaciones de ARO se mezclaron (q < 0.7) o se agruparon por separado en los dos nuevos grupos S3 y S4 (ARO7 y ARO12, respectivamente). Curiosamente, el tipo comercial MCO formó un racimo distinto (S5) separado de la cebolla roja de Apulia.
Relaciones genéticas entre poblaciones
El polimorfismo SSR permitió dibujar un dendrograma de diversidad genética y los resultados del análisis filogenético se muestran en la Figura 3a. Aquí, la colección de germoplasma se dividió en cinco grupos fuertemente respaldados por valores de arranque. Las poblaciones ARO7 y ARO12 se separaron inmediatamente de las poblaciones restantes y formaron dos grupos distintos. El tercer grupo incluía las dos poblaciones comerciales de TRO, mientras que el cuarto nodo dividía MCO de once poblaciones ARO. La relación genética que ocurre entre las poblaciones se investigó más a fondo mediante el análisis de coordenadas principales (PCoA) (Figura 3b). Como se destacó anteriormente, las poblaciones de ARO se agruparon estrechamente, excepto ARO12 y ARO7, que aparecieron en posiciones aisladas en el gráfico de PCoA. Las dos TRO y las poblaciones de MCO se dispersaron en el panel inferior derecho de la gráfica.
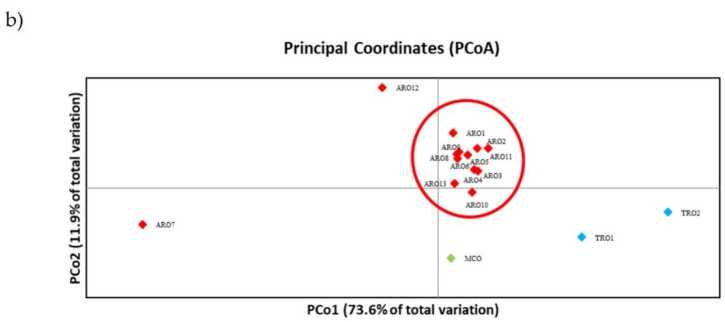
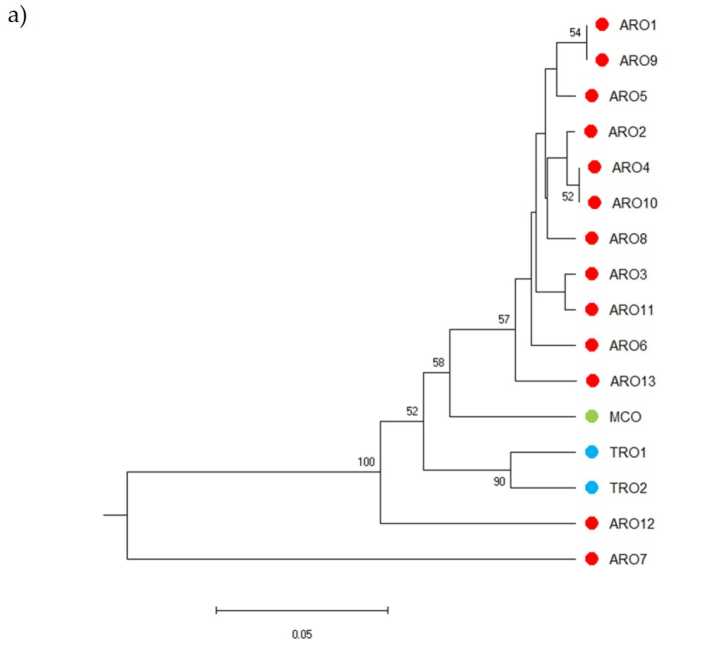
Figura 3. Diversidad genética entre 16 A cepa poblaciones caracterizadas en este estudio, en base a su perfil SSR. (a) Dendograma UPGMA de distancia genética. Los valores de soporte de Bootstrap >50 se indican encima de los nodos correspondientes; (b) análisis de componentes principales (PCoA). El grupo encerrado en un círculo rojo coincidía completamente con el grupo generado por el análisis filogenético y constituido por 11 accesiones ARO.
Discusión
Dentro de la gran cantidad de agrobiodiversidad cultivada tradicionalmente en el sur de Italia, las variedades locales de cebolla representan productos de nicho que deben preservarse del riesgo de erosión genética y la amenaza de reemplazo por cultivares modernos. En el marco del proyecto regional BiodiverSO, cuyo objetivo es recolectar, caracterizar, promover y salvaguardar los recursos genéticos de la región de Apulia fuertemente vinculados al patrimonio local, establecimos una colección de semillas de 13 poblaciones de la raza autóctona ARO. Reportamos la primera evaluación de la variación de ARO en términos de polimorfismos de ADN y dos parámetros bioquímicos, sólidos solubles y contenido de ácido pirúvico, relacionados con rasgos de sabor y de importancia para la aceptación de los productos frescos sin cocinar. Además, los datos de la variedad autóctona ARO se compararon con los recopilados en otras dos variedades autóctonas de cebolla pigmentada con las que a menudo se confunde.
Los análisis bioquímicos destacaron el dulzor de las 13 poblaciones ARO, relacionado con un alto contenido de sólidos solubles y una pungencia media, según las directrices de la industria de la cebolla dulce. [ 31 ]. Los bulbos ARO eran más dulces que los de las razas locales TRO y MCO, y mostraban una acritud ligeramente superior. Sin embargo, la dulzura en las cebollas se debe a un equilibrio entre el contenido de azúcar y la acritud, por lo que esta caracterización podría ser útil para apoyar la selección de genotipos de valor, que generalmente realizan los agricultores solo en función de la morfología.
Se confirmó que los marcadores SSR son una herramienta útil para discriminar genotipos, aunque se recolectaron dentro de un área de cultivo estrecha como la ciudad de Acquaviva delle Fonti. Los marcadores seleccionados mostraron un mayor número de alelos que los marcadores informados previamente por [ 43 ] y [ 44 ], pero inferior a los marcadores reportados por [ 45 ]. Además, el 50% de nuestro conjunto de marcadores mostró valores de índice PIC superiores a 0.5, demostrando ser adecuados para discriminar las poblaciones de la colección, como lo sugieren [ 46 ]. La evaluación de la diversidad dentro de las poblaciones reveló valores similares entre Ho y He, lo que resultó en un bajo Fis valores. Esto está de acuerdo con la naturaleza cruzada de A cepa, que sufre gravemente de depresión endogámica [ 47 ]. El Fi generals valor calculado en las poblaciones de cebolla consideradas en este estudio (0.054) fue inferior al reportado previamente por [ 45 ] (0.22) y casi idéntico al encontrado por [ 31 ] (0.08) y [ 48 ] (0.00) quienes evaluaron la diversidad genética en variedades locales de cebolla del noroeste de España y Níger, respectivamente. Los niveles notables de heterocigosidad en las poblaciones ARO refuerzan la idea de que Apulia representa un centro de diversidad para muchas especies hortícolas. [32, 42, 49-dieciséis].
AMOVA destacó que la mayor parte de la variación molecular en la colección genotipada en este estudio se encuentra dentro de las poblaciones. Sin embargo, la diferenciación genética significativa entre las poblaciones (FPT valores) revelaron la ocurrencia de estratificación genética. De hecho, aunque nuestros resultados indicaron la presencia de uniformidad genética en la mayoría de las poblaciones ARO, formando un grupo bien definido, las poblaciones ARO7 y ARO12 mostraron un perfil genético claramente diferenciado. Este resultado podría deberse a un origen diferente de las semillas utilizadas por los dos agricultores de los que se recolectaron las poblaciones. Además, en base a los resultados obtenidos, la raza ARO puede considerarse claramente distinta a nivel genético de las razas TRO y MCO. En un estudio reciente, [ 29 ] evaluó la diversidad genética de varias variedades locales de cebollas italianas, incluidas "Acquaviva", "Tropea" y "Montoro". Aunque los autores utilizaron marcadores SNP para evaluar la diversidad genética de una colección más amplia de cebollas, el genotipado no pudo discriminar las cebollas "Acquaviva" de las cebollas "Tropea" y "Montoro". Probablemente, esta discrepancia se deba al bajo valor medio de PIC encontrado (0.292), lo que sugiere una información general modesta de los loci bajo análisis, como afirman [ 29 ]. Además, para investigar la presencia de subestructura en su grupo italiano, hubiera sido mejor analizar los genotipos italianos por separado del resto de la colección. Probablemente hubiera permitido visualizar patrones de diversidad genética ligados a estratificación geográfica o rasgos bajo selección empírica.
En conclusión, el presente estudio representa un informe completo sobre una variedad local de cebolla asociada con el patrimonio cultural local y de importancia económica para los agricultores. Nuestros resultados destacan que, con algunas excepciones, ARO se caracteriza por un acervo genético bien definido, que merece ser preservado del riesgo de erosión genética. Por lo tanto, el establecimiento de una colección representativa de esta valiosa fuente de diversidad genética ha sido crucial. Finalmente, la caracterización genética y fenotípica de ARO podría ser útil para obtener marcas de calidad de la Unión Europea.
Materiales y Métodos
Recolección de germoplasma, material vegetal y extracción de ADN
Se adquirió un conjunto de 13 poblaciones de la variedad autóctona ARO en el marco de un proyecto de la región de Apulia (BiodiverSO: https://www.biodiversitapuglia.it/), a través de una serie de misiones realizadas en “Acquaviva delle Fonti”, un pequeño pueblo de Apulia en la Provincia de Bari, Italia. Los sitios de recolección de cada accesión se mapearon a través del Sistema de Información Geográfica (SIG) y se reportaron en la Tabla 4. Además, dos poblaciones de la raza local TRO y una población de la raza local MCO se incluyeron en el presente estudio y se usaron como referencias. Todo el material vegetal fue cultivado en las mismas condiciones ambientales en la finca experimental “P Martucci” de la Universidad de Bari (41° 1'22.08″ N, 16°54'25.95″ E), bajo jaula de protección para evitar la polinización cruzada entre poblaciones y asegurando la polinización intrapoblacional por medio de moscas azules (Lucilia César). Las 16 poblaciones se caracterizaron por rasgos relacionados con el tamaño y la forma del bulbo y el color de la piel y la pulpa (Tabla S1). Además, se realizó un ensayo de contenido de sólidos solubles usando un refractómetro de mano y se midió la acritud en muestras de jugo de cebolla agregando 2,4-dinitrofenilhidrazina (0.125% v/v en 2N de HCl) y evaluando la absorbancia a 420 nm, según lo informado por [ 31 ]. Se realizó la prueba de rangos múltiples de Duncan y la prueba de SNK para determinar la presencia de diferencias significativas.
Tabla 4. Lista de poblaciones recolectadas y genotipadas en este estudio. Para cada Población se reporta Código de Identificación, Nombre Local, Coordenada GPS y Banco de Genes que Preserva las Semillas.
| Código | Nombre | Coordenadas GPS | Banco de genes y |
| ARO1 | Cipolla roja de Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla roja de Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla roja de Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla roja de Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla roja de Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla roja de Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla roja de Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla roja de Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla roja de Acquaviva | 40°54"51.372″ N 16°49"3.504" E | Di.SSPA |
| ARO10 | Cipolla roja de Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla roja de Acquaviva | 40°52"49.8″ N 16°49"48.575" E | Di.SSPA |
| ARO12 | Cipolla roja de Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla roja de Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla roja pulmonada de Tropea | – | Di.SSPA |
| TRO2 | Cipolla roja tonda di Tropea | – | Di.SSPA |
| MCO | Cipolla ramata de Montoro | – | Di.SSPA |
| y Di.SSPA, Departamento de Ciencias del Suelo, Plantas y Alimentos, Universidad de Bari. |
Se tomaron muestras de material foliar de 20 genotipos por población y se almacenaron a -80 °C hasta su uso. Para especies ricas en polisacáridos, como A cepa, Los primeros pasos para eliminar el polisacárido son esenciales para obtener ADN de buena calidad, por lo que se realizaron lavados iniciales en tampón STE (sacarosa 0.25 M, Tris 0.03 M, EDTA 0.05 M) como se describe por [ 52 ]. El ADN total se extrajo siguiendo el método CTAB [ 53 ] y finalmente se verificó su calidad y concentración mediante espectrofotómetro UV-vis Nano Drop 2000 (ThermoScientific, Waltham, MA, EE. UU.) y electroforesis en gel de agarosa al 0.8%.
Análisis RSS
16 combinaciones de cebadores EST-SSR desarrolladas por [ 54 ] y probado previamente en estudios de diversidad genética por [ 43 ] y [ 44 ] y 21 SSR genómico [45-dieciséis] fueron examinados para evaluar su idoneidad (Tabla complementaria S4). El genotipado se realizó utilizando el método de etiquetado fluorescente económico en el que la cola M13 se agrega a cada cebador SSR directo. [ 56 ]. Las mezclas de PCR se prepararon en 20 gL de reacción que contenían: 50 ng de ADN total, 0.2 mM de mezcla de dNTP, 1X de tampón de reacción de PCR, 0.8 U de ADN polimerasa DreamTaq (Thermo Scientific, Waltham, MA, EE. UU.), 0.16 gM de cebador inverso , 0.032 gM de cebador directo extendido con la secuencia M13 (5′-TGTAAAACGACGGCCAGT-3′) y 0.08 gM de un cebador universal M13 marcado con colorantes fluorescentes FAM o NED (Sigma-Aldrich, St. Louis, MO, EE. UU.). Las reacciones de PCR se llevaron a cabo en el termociclador SimpliAmp (Applied Biosystems, CA, EE. UU.) con las siguientes condiciones para la mayoría de los pares de cebadores: 94 °C durante 5 min, 40 ciclos a 94 °C durante 30 s, 58 °C por 45 s y 72 °C por 45 s y una elongación final a 72 °C por 5 min. En cuanto a ACM446 y ACM449, se aplicó una PCR de contacto con hibridación de 60 °C a 55 °C durante 10 ciclos, 30 ciclos a 55 °C, seguido de una extensión final de 5 min a 72 °C. Los productos de PCR se cargaron en una placa de 96 pocillos y se mezclaron con 14 gL de Hi-Di Formamide (Life Technologies, Carlsbad, CA, EE. UU.) y 0.5 gL de GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, EE. UU.). Los amplicones se resolvieron mediante una máquina de secuenciación capilar ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, EE. UU.), donde los alelos se calificaron como co-dominantes y se asignaron mediante el software GeneMapper, versión 3.7.
Los programas GenAlEx 6.5 [ 57 ] y Cervus 3.0.7 [ 58 ] se utilizaron para estimar el número de alelos (Na), el número de alelos efectivos (Ne), la heterocigosidad observada (Ho), la heterocigosidad esperada (He), el contenido de información polimórfica (PIC), el índice de información de Shannon (I) y el índice de fijación (Fis ) para cada locus SSR.
Evaluación de la Diversidad Genética
La partición jerárquica de la variación genética entre y dentro de las poblaciones de cebolla fue evaluada por GenAlEx 6.5 [ 57 ] a través del análisis de varianza molecular (AMOVA) con bootstrapping 999 para probar la significancia. Además, se utilizó el software GenAlEx 6.5 para estimar la diversidad dentro de cada población calculando el promedio de Ho, He y Fis en todos los loci SSR.
La estructura de la población se infirió mediante el algoritmo de agrupamiento basado en el modelo bayesiano implementado en el software STRUCTURE v.2.3.4 [ 59 ]. El conjunto de datos se ejecutó con una cantidad de grupos hipotéticos (K), que van del 1 al 10, estableciendo diez ejecuciones independientes para cada valor de K. Para cada ejecución, con el objetivo de verificar la consistencia de los resultados, se realizaron 100,000 100,000 iteraciones del período de quemado inicial y XNUMX XNUMX cadenas de Markov Monte Carlo (MCMC) bajo el modelo de mezcla y frecuencias alélicas independientes entre las poblaciones. El valor de K más probable se determinó implementando el método AK, descrito por [ 60 ], en el programa web STRUCTURE HARVESTER [ 61 ]. Una población individual se asignó a un conglomerado específico cuando su coeficiente de pertenencia (valor q) fue superior a 0.7; de lo contrario, se consideró de ascendencia mixta.
Se realizó un análisis de coordenadas principales para visualizar patrones de relación genética entre las accesiones reveladas por la matriz de distancia genética de Nei (Tabla complementaria S5). Con base en las frecuencias alélicas, se construyó un dendrograma de distancia genética implementando el método de grupos de pares no ponderados con análisis de conglomerados de promedios aritméticos (UPGMA) en el software POPTREEW [ 62 ]. Se aplicó Bootstrapping para evaluar la confianza en el agrupamiento jerárquico, estableciendo 100 remuestreos del conjunto de datos. Finalmente, el software MEGA X [ 63 ] se utilizó como software de dibujo de árboles.
Materiales complementarios: Los siguientes están disponibles en línea en http://www.mdpi.com/2223-7747/9/2/260/s1. Tabla S1: Caracterización morfológica de los bulbos ARO, MCO y TRO. Tabla S2: Heterocigosidad e índices de fijación calculados para variedades locales ARO y variedades locales TRO y MCO. Tabla S3: Valores por pares del parámetro Fpt. Tabla S4: Lista de los SSR utilizados en el estudio. Tabla S5. Matriz de población por pares de distancia genética Nei. Figura S1: gráfico de líneas de valores K que cambian con Delta K de Evanno.
Contribuciones de autor: CL y LR concibieron el estudio y diseñaron el experimento; CL y PI realizaron análisis de marcadores moleculares; ARM y VZ realizaron las pruebas de campo; RM, SP, GR y CL participaron en el análisis de datos; RM y CL escribieron el manuscrito. Todos los autores han leído y aceptado la versión publicada del manuscrito.
Fondos: Este trabajo fue financiado por el proyecto regional de Apulia “Biodiversidad de especies vegetales de Apulia”—Programma di Sviluppo Rurale per la Puglia 2014-2020. Misura 10—Sottomisura 10.2; subvención CUP H92C15000270002, Italia.
Expresiones de gratitud: Se agradece a la “Azienda Agricola Iannone Anna” y a la “Associazione produttori della vera cipolla rossa di Acquaviva” por proporcionar los materiales vegetales utilizados en el experimento.
Conflictos de interés: Los autores declaran no tener conflicto de intereses.
Referencias
- 1. Stearn, WT ¿Cuántas especies de Allium se conocen? Mag. Kew. 1992, 9180-182. [CrossRef]
- 2. FAOSTAT. Base de datos estadísticos de la FAO. Disponible en linea: http://www.fao.org/2017 (accedido en 8 enero 2019).
- 3. Block, E. La química del ajo y la cebolla. Sci. A.m. 1985, 252114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Evaluación de la cebolla roja sobre la actividad antioxidante en ratas. Química alimentaria Toxicol. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Luna, J.; Chung, JH; Cha, YJ; Shin, MJ Efecto de los extractos de cáscara de cebolla ricos en quercetina sobre la trombosis arterial en ratas. Química alimentaria Toxicol. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Efectos contra la obesidad del extracto de cebolla en ratas grasas diabéticas zucker. Nutrientes 2012, 4,1518-1526. [CrossRef]
- 7. Akasha, MSH; Rehman, K.; Chen, S. Spice plant Allium cepa: Suplemento dietético para el tratamiento de la diabetes mellitus tipo 2. Nutrición 2014, 301128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Efectos inhibidores de la cebolla (Allium cepa L.) sobre la proliferación de células cancerosas y adipocitos a través de la inhibición de la sintasa de ácidos grasos. Pac asiático. J. Cáncer Anterior. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, Carolina del Sur; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Lien, JC; Tsai, CH; Chung, JG La quercetina inhibe la migración y la invasión de células cancerosas orales humanas SAS a través de la inhibición de las vías de señalización de NF-kappaB y metaloproteinasa de matriz-2/-9. Anticancer Res. 2013, 331941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Ajo y cebolla: sus propiedades de prevención del cáncer. Cáncer Prev. Res. 2015, 8,181-189. [CrossRef]
- 11. Fuerte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Propiedades antioxidantes y de reparación ósea de la hidroxiapatita funcionalizada con quercetina: un estudio in vitro de cocultivo de células endoteliales de osteoblastos y osteoclastos. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Distribución de once precursores de sabor, derivados de S-Alk (en) il-L-cisteína, en siete vegetales Allium. ciencia de la comida Tecnología Res. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. La química de los organosulfuros del género Allium: implicaciones para la química orgánica del azufre. Angew. Chem. En t. Ed. Engl. 1992, 311135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Tomás, B.; Smith, B. Cebollas: un beneficio global para la salud. fitotera. Res. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Desarrollo enzimático de ácido pirúvico en cebolla como medida de acritud. J. Agric. Química alimentaria 1961, 9, 301-304. [CrossRef]
- 16. Ketter, CAT; Randle, WM Evaluación de pungencia en cebollas. En Estudios Probados para la Enseñanza de Laboratorio; Karcher, SJ, Ed.; Asociación para la Educación en Laboratorios de Biología (ABLE): Nueva York, NY, EE. UU., 1998; Tomo 19, págs. 177-196.
- 17. Hanelt, P Taxonomía, evolución e historia. En Cebollas y cultivos afines, vol. I. Botánica, Fisiología y Genética; Rabinowitch, HD, Brewster, JL, Eds.; CRC Press: Boca Ratón, FL, EE. UU., 1990; págs. 1-26.
- 18. Rabinowitch, HD; Curra, L. Allium Crop Science: avances recientes; CABI Publishing: Wallingford, Reino Unido, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. Caracterización de recursos genéticos de cebolla. (Allium cepa L.) del centro de secundaria español de la diversidad. Lapso. J. Agric. Res. 2011, 9144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Evaluación de fenoles y sulfóxidos de cisteína en germoplasma local de cebolla y chalote de Italia y Ucrania. Gineta. recurso Cultivo Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernández, A.; Barros, L.; Ferreira, SCIIF; Ntatsi, G. Descripción morfológica, nutricional y química de 'vatikiotiko', una raza local de cebolla de Grecia. Química alimentaria 2015,182156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazaro, F.; Fratianni, F.; Di Mateo, M.; Albanese, D. Propiedades bioquímicas, antioxidantes y actividad antimicrobiana de diferentes variedades de cebolla en el área mediterránea. J. Medición de alimentos. carácter 2019,131232-1241. [CrossRef]
- 23. Yoo, KS; Lucio, L.; Crosby, K.; Jones, R.; Leskovar, D. Diferencias en la pungencia de la cebolla debido a los cultivares, el entorno de crecimiento y los tamaños de los bulbos. ciencia Hortico. 2006,110144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; Jorge, E.; Kroh, LW; Rohn, S. Distribución de quercetina-3, 4′-O-diglucósido, quercetina-4′-O-monoglucósido y quercetina en diferentes partes del bulbo de cebolla (Allium cepa L.) influenciada por el genotipo. Química alimentaria 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villarí, G.; Borrelli, C.; Melchonna, G.; Minutolo, M.; Ruso, G.; Amalfitano, C. Efectos de la época de trasplante y la densidad de plantación sobre el rendimiento, la calidad y el contenido de antioxidantes de la cebolla (Allium cepa L.) en el sur de Italia. ciencia Hortico. 2014,166111-120. [CrossRef]
- 26. Pérez-Gregorio, MR; Regueiro, J.; Simal-Gándara, J.; Rodríguez, AS; Almeida, DPF Incrementando el valor agregado de las cebollas como fuente de flavonoides antioxidantes: Una revisión crítica. Crit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. Impacto del método de cultivo y selección de cultivares en carbohidratos solubles y principios picantes en cebollas (Allium cepa l.). J. Agric. Química alimentaria 2018, 6612827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Identificación y cuantificación de flavonoides de dos cultivares del sur de Italia de Allium cepa L., Tropea (cebolla roja) y Montoro (cebolla cobre), y su capacidad para proteger los eritrocitos humanos del estrés oxidativo. J. Agric. Química alimentaria 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Espósito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. El genotipado de alto rendimiento en cebolla revela la estructura de la diversidad genética y los SNP informativos útiles para el mejoramiento molecular. mol. Raza. 2019, 39, 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Variación genética de un tomate italiano de larga vida útil (Solanum lycopersicum L.) colecta mediante SSR y caracteres morfológicos del fruto. Gineta. recurso Cultivo Evol. 2014, 62, 721-732. [CrossRef]
- 31. González-Pérez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. Explorando la diversidad genética y los rasgos de calidad en una colección de cebolla (Allium cepa L.) variedades autóctonas del noroeste de España. Genética 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Ioviano, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Sumo, C.; Paván, S.; Ricciardi, L. Caracterización genética, bioagronómica y nutricional de la col rizada (Brassica oleracea L.var. acéfala) diversidad en Apulia, sur de Italia. Diversidad 2018,10, 25. [CrossRef]
- 33. Bárdaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Paván, S.; Ricciardi, L. Análisis genético de la resistencia a Orobanche crenata (Tenedor.) en un guisante (Pisum sativum L.) línea de baja estrigolactona. J. Plant Pathol. 2016, 98, 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Mapeo de loci de rasgos cuantitativos para el tiempo de floración en racimos de cebolla (Allium fistulosum l.). eufítica 2016, 209, 537-546. [CrossRef]
- 35. Dhaka, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pental, D.; Pradhan, AK Identificación de SSR génicos y construcción de un mapa de ligamiento basado en SSR en Brassica juncea. eufítica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. Evaluación de la identidad varietal de cebolla utilizando marcadores SSR. ciencia de semillas Tecnología 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. Selección y validación de un conjunto de marcadores para la diferenciación de cultivares de cebolla de la República Checa. Checo J. Genet. Raza vegetal. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. La conservación y caracterización de la biodiversidad del germoplasma de olivo de Apulia. Acta Hortica. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andrés, A.; Garces-Claver, A. Evaluación de la diversidad genética del español Allium cepa variedades locales para el mejoramiento de cebolla utilizando marcadores microsatélites. ciencia Hortico. 2014,17024-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; García-Ulloa, A.; Pomar, F.; Silvar, C. Evaluación de la diversidad genética en cebolla (Allium cepa L.) variedades locales del noroeste de España y comparación con la variabilidad europea. Cultivo NZJ Hortic. 2016, 44103-120. [CrossRef]
- 41. De Giovanni, C.; Paván, S.; Tarento, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Variación genética de una colección global de germoplasma de garbanzo (Cicer arietinum L.), incluidas las accesiones italianas en riesgo de erosión genética. Fisiol. mol. Biol. Plantas 2017, 23197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Paván, S.; Ricciardi, L.; Lotti, C. Diversidad genética en brócoli rabe (Brassica rapa L. subesp. Sylvestris (L.) Janch.) del sur de Italia. ciencia Hortico. 2019, 253140-146. [CrossRef]
- 43. Jakse, M.; Martín, W.; McCallum, J.; Havey, M. Polimorfismos de un solo nucleótido, indeles y repeticiones de secuencias simples para la identificación de cultivares de cebolla. Mermelada. Soc. Hortico. ciencia 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Análisis de diversidad genética y desarrollo de marcadores de polimorfismo de un solo nucleótido en cebollas de bulbo cultivadas basado en marcadores repetidos de secuencia simple de etiqueta de secuencia expresada. Mermelada. Soc. Hortico. ciencia 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Desarrollo de marcadores de repetición de secuencia simple genómicos robustos para la estimación de la diversidad genética dentro y entre cebollas de bulbo (Allium cepa L.) poblaciones. mol. Raza. 2012, 301401-1411. [CrossRef]
- 46. De Woody, JA; Honeycutt, RL; Marcadores Skow, LC Microsatellite en venado cola blanca. J. Hered. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. cebolla iraní (Allium cepa L.) respuestas de cultivares a la depresión endogámica. aplicación mundial ciencia j 2010,11, 426-428.
- 48. Abdu, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Diversidad genética de las cebollas de Níger (Allium cepa L.) evaluado por marcadores de repetición de secuencia simple (SSR). Acta Hortica. 2016,1143, 77-90. [CrossRef]
- 49. Paván, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bárdaro, N.; Bracuto, V.; Ricciardi, F.; Tarento, F.; D'Agostino, N.; Schiavulli, A.; et al. Un grupo genético distinto en el garbanzo cultivado como lo revela el descubrimiento de marcadores de todo el genoma y la genotipificación. genoma vegetal 2017, 2017,10. [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Genotipado por secuenciación de un melón (Cucumis melo L.) la colección de germoplasma de un centro secundario de diversidad destaca patrones de variación genética y características genómicas de diferentes acervos genéticos. Genoma BMC. 2017, 18, 59. [CrossRef]
- 51. Di Rienzo, V.; Sión, S.; Tarento, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Pasqualone, A.; et al. Flujo genético entre la población de olivos en la cuenca mediterránea. compañero j 2018, 6. [CrossRef]
- 52. Pastor, LD; McLay, TG Dos protocolos a microescala para el aislamiento de ADN de tejido vegetal rico en polisacáridos. Planta J. Res. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Aislamiento de ADN vegetal a partir de tejido fresco. Focus 1990,1213-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martín, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Fregadero, KC; Jenderek, M.; et al. Un conjunto único de 11,008 etiquetas de secuencias expresadas en cebolla revela secuencias expresadas y diferencias genómicas entre los órdenes de monocotiledóneas asparagales y poales. Célula vegetal 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, recursos humanos; Hyun, JY; Canción, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Desarrollo de marcadores para pruebas de pureza genética de cebolla utilizando SSR Finder. Corea J. Raza. ciencia 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Un método económico para el etiquetado fluorescente de fragmentos de PCR. Nat. Biotecnología 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Análisis genético en Excel. Software de genética de poblaciones para la enseñanza y la investigación: una actualización. Bioinformática 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; cónica, ML; Marshall, TC Revisar cómo el programa de computadora CERVUS acomoda el error de genotipado aumenta el éxito en la asignación de paternidad. mol. Ecol. 2007,161099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Mapeo de asociaciones en poblaciones estructuradas. Soy. J. Hum. Gineta. 2000, 67, 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Detectando el número de conglomerados de individuos usando el software ESTRUCTURA: Un estudio de simulación. mol. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61. Conde, D.; VonHoldt, B. STRUCTURE HARVESTER: un sitio web y un programa para visualizar la salida de STRUCTURE e implementar el método Evanno. Conservar Gineta. recurso 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: versión web de POPTREE para construir árboles de población a partir de datos de frecuencia de alelos y calcular algunas otras cantidades. mol. Biol. Evol. 2014, 31, 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Análisis genético evolutivo molecular en plataformas informáticas. mol. Biol. Evol. 2018, 351547-1549. [CrossRef]